Solid
| Part of a series on |
| Continuum mechanics |
|---|
| Condensed matter physics |
|---|
 |

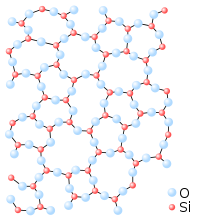
고체(Solid)는 물질의 네 가지 기본 상태(four fundamental states of matter) 중 하나입니다 (다른 것은 액체(liquid), 기체(gas), 및 플라즈마(plasma)가 있습니다). 고체에서 분자는 서로 밀집되어 있고 최소한의 운동 에너지를 포함합니다. 고체는 구조적 강성(structural rigidity)과 표면에 가해지는 힘에 대한 저항에 의해 특징짓습니다. 액체와 달리, 단단한 대상은 그의 용기의 모양을 취하기 위해 흐르지 않고, 기체처럼 그것에 대해 사용 가능한 전체 부피를 채우기 위해서 확대되지도 않습니다. 고체에서 원자는 규칙적 기하학 격자(geometric lattice) (금속과 보통의 얼음을 포함하는 수정 고체(crystalline solids)), 또는 불규칙적으로 (공통적인 창유리와 같은 무정형성 고체(amorphous solid))을 포함하는 서로 단단히 결합됩니다. 고체는 작은 압력으로는 압축될 수 없고 반면에 기체에서 분자는 느슨하게 포장되기 때문에 작은 압력으로 압축될 수 있습니다.
고체를 다루는 물리학의 분야는 고체-상태 물리학(solid-state physics)이라고 불리고, (액체도 역시 포함하는) 응축된 물질 물리학(condensed matter physics)의 주요 분야입니다. 재료 과학(materials science)은 주로 고체의 물리적(physical) 및 화학적 속성(chemical properties)과 관련됩니다. 고체-상태 화학은 신소재의 합성(synthesis)뿐만 아니라, 식별 및 화학 성분(chemical composition)의 과학에 특히 중점을 둡니다.
Microscopic description

고체를 구성하는 원자, 분자, 또는 이온은 규칙적으로 반복되는 패턴으로 배열되거나 불규칙하게 배열될 수 있습니다. 구성 성분이 규칙적인 패턴으로 배열된 물질은 결정(crystals)이라고 알려져 있습니다. 일부 경우에서, 각 다이아몬드가 단일 결정(single crystal)인 다이아몬드와 같이 대규모에 걸쳐 규칙적인 순서가 깨지지 않고 계속될 수 있습니다. 보고 다룰 수 있을 만큼 큰 고체 물체는 단일 결정으로 구성되는 경우가 거의 없지만, 대신 크기가 수 나노미터에서 수 미터까지 다양할 수 있는 결정자(crystallites)로 알려진 것은 많은 수의 단일 결정으로 구성됩니다. 그러한 재료는 다결정(polycrystalline)이라고 불립니다. 거의 모든 공통적인 금속과 많은 세라믹(ceramics)은 다결정입니다.
다른 재료에서, 원자의 위치에 긴 범위의 순서가 없습니다. 이들 고체는 무정형 고체(amorphous solids)로 알려져 있습니다; 예로는 폴리스티렌(polystyrene)과 유리가 있습니다.
고체가 결정자인지 무정형인지는 관련된 재료와 그것이 형성되는 조건에 따라 다릅니다. 느린 냉각에 의해 형성된 고체는 결정자가 되는 경향이 있는 반면, 빠르게 동결된 고체는 무정형일 가능성이 더 큽니다. 마찬가지로, 결정자 고체에 의해 채택된 특정 결정 구조(crystal structure)는 포함된 물질과 형성 방법에 따라 달라집니다.
얼음 정육면체이나 동전과 같은 많은 공통적인 물체는 전체적으로 화학적으로 동일하지만, 많은 다른 공통적인 물질은 함께 포장된 여러 가지 다른 물질로 구성됩니다. 예를 들어, 전형적인 암석은 특정 화학 성분을 가지지 않는 여러 가지 광물과 광물성 물질의 집합체입니다. 목재는 주로 유기 리그닌 매트릭스에 포함된 셀룰로오스 섬유로 구성된 천연 유기 재료입니다. 재료 과학에서 하나 이상의 구성 재료로 구성된 복합 재료는 원하는 속성을 갖도록 설계될 수 있습니다.
Classes of solids
고체에서 원자 사이의 힘은 다양한 형식을 취할 수 있습니다. 예를 들어, 염화나트륨 (일반적인 소금)의 결정은 이온 결합(ionic bonds)에 의해 함께 유지되는 이온성 나트륨과 염소로 구성됩니다.[1] 다이아몬드 또는 실리콘에서,[2] 원자는 전자를 공유하고 공유 결합(covalent bonds)을 형성합니다.[3] 금속에서, 전자는 금속 결합(metallic bonding)에서 공유됩니다.[4] 일부 고체, 특히 대부분의 유기 화합물은 각 분자에서 전자 전하 구름의 분극화로 인해 발생하는 반 데르 발스 힘(van der Waals forces)과 함께 유지됩니다. 고체 유형 사이의 차이점은 결합의 차이에서 비롯됩니다.
Metals

금속은 전형적으로 강하고, 조밀하고, 전기와 열의 좋은 전도체입니다.[5][6] 주기율 테이블에서 붕소에서 폴로늄으로 이어지는 대각선의 왼쪽에 있는 대부분의 원소는 금속입니다. 주성분이 금속인 둘 이상의 원소의 혼합물은 합금(alloys)이라고 알려져 있습니다.
사람들은 선사 시대부터 다양한 목적으로 금속을 사용해 왔습니다. 금속의 강도와 신뢰성으로 인해 대부분의 차량, 많은 기계 기구와 도구, 파이프, 도로 표지판과 철도 트랙뿐만 아니라 건물과 기타 구조물의 건설에 널리 사용되어 왔습니다. 철과 알루미늄은 가장 공통적으로 사용되는 두 가지 건축의 금속입니다. 그것들은 역시 지구의 지각(Earth's crust)에서 가장 풍부한 금속입니다. 철은 최대 2.1%의 탄소(carbon)를 포함하는 합금인 강철의 형태로 가장 공통적으로 사용되며, 순수한 철보다 훨씬 더 단단합니다.
금속은 전기가 잘 통하는 전도체이기 때문에, 그것들은 전기 제품과 에너지 손실이나 손실이 거의 없이 장거리에 걸쳐 전류를 운반하는 데 유용합니다. 따라서, 전기 파워 격자는 전기를 분배하기 위해 금속 케이블에 의존합니다. 예를 들어, 가정용 전기 시스템은 우수한 전도 속성과 용이한 가공성을 위해 구리로 배선됩니다. 대부분의 금속은 열전도율이 높기 때문에 스토브탑 조리 기구에 유용합니다.
금속 원소와 그 합금에 대한 연구는 고체-상태 화학, 물리학, 재료 과학, 및 공학 분야의 상당 부분을 차지합니다.
금속 고체는 "금속 결합"으로 알려진 높은 밀도의 공유된, 지역화되지 않은 전자에 의해 함께 유지됩니다. 금속에서, 원자는 가장 바깥쪽("가") 전자를 쉽게 잃어, 양 이온(ions)을 형성합니다. 자유 전자는 전체 고체에 걸쳐 퍼져 있으며, 이는 이온과 전자 구름 사이의 정전기적 상호 작용에 의해 단단히 고정됩니다.[7] 많은 수의 자유 전자(free electrons)는 금속에 높은 값의 전기와 열 전도성을 제공합니다. 자유 전자는 역시 가시반직선의 투과를 방지하여 금속을 불투명하고 광택이 나도록 만듭니다.
보다 발전된 금속 속성 모델은 지역화되지 않은 전자에 대한 양 이온 코어의 영향을 고려합니다. 대부분의 금속은 결정 구조를 가지므로, 그것들의 이온은 보통 주기적 격자로 배열됩니다. 수학적으로, 이온 코어의 퍼텐셜은 다양한 모델로 처리할 수 있으며, 가장 간단한 것은 거의 자유 전자 모델(nearly free electron model)입니다.
Minerals

광물은 높은 압력 아래에서 다양한 지질학적 과정을 통해 형성된 자연적으로 발생하는 고체입니다.[8] 진정한 광물로 분류되기 위해, 물질이 전체적으로 균등한 물리적 속성을 갖는 결정 구조(crystal structure)를 가져야 합니다. 광물은 순수한 원소(pure elements)와 단순한 염(salts)에서 수천 가지의 알려진 형태를 갖는 매우 복잡한 규산염(silicates)에 이르기까지 그 구성 범위가 다양합니다. 대조적으로, 암석 표본은 광물 및/또는 광물류(mineraloid)의 무작위 집합체이고, 특정 화학 조성이 없습니다. 지구의 지각(Earth's crust) 암석의 대부분은 석영 (결정질의 SiO2), 장석, 운모, 녹니석, 카올린, 방해석, 에피도트, 감람석, 오자이트, 각섬석, 자철광, 적철광, 갈철광, 및 기타 몇 가지 광물로 구성됩니다. 석영, 운모, 또는 장석과 같은 일부 광물은 공통적이지만, 다른 광물은 전 세계적으로 몇 군데에서만 발견되어 왔습니다. 지금까지 가장 큰 광물 그룹은 규산염 (대부분의 암석은 규산염이 95% 이상임)으로, 주로 규소와 산소로 구성되며, 알루미늄, 마그네슘, 철, 칼슘, 및 기타 금속 이온이 추가됩니다.
Ceramics

세라믹 고체는 무기 화합물, 보통 화학 원소의 산화물(oxides)로 구성됩니다.[9] 그것들은 화학적으로 불활성이고, 종종 산성 또는 부식성의 환경에서 발생하는 화학적 침식을 견딜 수 있습니다. 세라믹은 일반적으로 1000에서 1600°C (1800에서 3000°F)의 높은 온도를 견딜 수 있습니다. 질화물(nitrides), 붕소화물(borides), 및 탄화물(carbides)과 같은 비-산화물 무기 재료는 예외입니다.
전통적인 세라믹 원료에는 카올리나이트와 같은 점토 광물이 포함되며, 최근에는 산화 알루미늄 (알루미나)이 포함됩니다. 고급 세라믹으로 분류되는 현대 세라믹 재료에는 실리콘 카바이드(silicon carbide)와 텅스텐 카바이드(tungsten carbide)가 포함됩니다. 둘 다 내마모성으로 인해 가치가 높았고, 따라서 광산 작업에서 분쇄 장비의 마모판과 같은 용도로 사용됩니다.
알루미나와 그 화합물과 같은 대부분의 세라믹 재료는 미세 분말로 형성되어, 가시반직선의 파장에 필적하는 광산란(light-scattering) 중심으로 채워진 미세 입자 다결정(polycrystalline) 미세-구조(microstructure)를 생성합니다. 따라서, 그것들은 투명 재료(transparent materials)와 달리 일반적으로 불투명 재료입니다. 최근의 나노-스케일 (예를 들어, 졸-겔) 기술은 높은-파워 레이저와 같은 응용 분야를 위한 투명 알루미나와 알루미나 화합물과 같은 다결정 투명 세라믹의 생산을 가능하게 했습니다. 고급 세라믹은 의료, 전기 및, 전자 산업에서도 사용됩니다.
세라믹 공학은 고체-상태 세라믹 재료, 부품, 및 장치를 만드는 과학과 기술입니다. 이것은 열의 작용에 의해, 또는, 더 낮은 온도에서, 화학 용액으로부터 침전 반응(precipitation reactions)을 사용하여 수행됩니다. 그 용어에는 원료의 정제, 관련 화합물의 연구와 생산, 구성 요소로의 형성, 구조, 구성, 및 속성에 대한 연구가 포함됩니다.
기계적으로 말하면, 세라믹 재료는 부서지기 쉽고, 단단하고, 압축에 강하고, 전단과 인장에 약합니다. 부서지기 쉬운(Brittle) 재료는 정적 하중을 지지함으로써 상당한 인장 강도(tensile strength)를 나타낼 수 있습니다. 인성(Toughness)은 기계적 고장 전에 재료가 흡수할 수 있는 에너지의 양을 나타내고, 반면에 파괴 인성(fracture toughness, KIc로 표시됨)은 균열 성장과 전파를 통해 파괴에 저항하는 고유한 미세-구조적 결함을 갖는 재료의 능력을 나타냅니다. 만약 재료의 파괴 인성 값이 크면, 파괴 역학의 기본 원리는 연성 파괴를 겪을 가능성이 가장 높다고 제안합니다. 부서지기 쉬운 파괴는 전형적으로 낮은 (및 비-일관된) KIc 값을 나타내는 대부분의 세라믹과 유리-세라믹 재료의 특징입니다.
세라믹 응용 분야의 예를 들어, 지르코니아(zirconia)의 극던적인 경도는 칼날과 기타 산업용 절단 도구의 제조에 활용됩니다. 알루미나, 탄화붕소, 및 탄화규소와 같은 세라믹은 대구경 라이플의 화재를 격퇴하기 위해 방탄조끼에 사용되어 왔습니다. 질화규소 부품은 높은 경도로 인해 내마모성이 있는 세라믹 볼 베어링에 사용됩니다. 일반적으로, 세라믹은 내화학성도 있고 강철 베어링이 산화되기 (또는 녹) 쉬운 습한 환경에서 사용할 수 있습니다.
세라믹 적용의 또 다른 예로서, 1980년대 초에, 토요타(Toyota)는 작동 온도가 6000°F (3300°C) 이상인 단열 세라믹 엔진의 생산을 연구했습니다. 세라믹 엔진은 냉각 시스템이 필요하지 않고 따라서 무게를 크게 줄일 수 있고 따라서 연료 효율이 높아집니다. 기존의 금속 엔진에서, 금속 부품의 멜트다운을 방지하기 위해 연료에서 방출되는 많은 에너지를 폐열로 소산해야 합니다. 가스 터빈 엔진용 세라믹 부품 개발 연구도 진행 중입니다. 세라믹으로 만든 터빈 엔진은 보다 효율적으로 작동할 수 있어, 항공기가 일정량의 연료에 대해 더 넓은 범위와 탑재량을 제공할 수 있습니다. 어쨌든, 그러한 엔진은 충분한 정밀도와 내구성으로 세라믹 부품을 제조하는 것이 어렵고 비용이 많이 들기 때문에 생산되지 않습니다. 처리 방법은 종종 소결 공정에서 자주 유해한 역할을 하는 미세한 결함의 광범위한 분포를 초래하여 균열 확산과 궁극적인 기계적 결함을 초래합니다.
Glass ceramics

유리-세라믹 재료는 비-결정질 유리와 결정질 세라믹 둘 다를 갖는 많은 속성을 공유합니다. 그것들은 유리로 형성되고, 그런-다음 열처리에 의해 부분적으로 결정화되어, 결정질 극미량이 비-결정질 입계 상 내에 삽입되도록 무정형 및 결정 상을 모두 생성합니다.
유리-세라믹은 열 충격에 대한 높은 저항성과 액체에 대한 극단적으로 낮은 침투성을 모두 가지는 조리기구 (원래 CorningWare라는 브랜드 이름으로 알려짐)와 스토브탑을 만들기 위해 사용됩니다. 결정질 세라믹 상의 음의 열팽창 계수는 유리질 상의 양의 계수와 균형을 이룰 수 있습니다. 특정 지점 (~70% 결정질)에서 유리-세라믹은 영에 가까운 순 열팽창 계수를 가집니다. 이 유형의 유리-세라믹은 우수한 기계적 속성을 나타내고 최대 1000°C까지 반복적이고 빠른 온도 변화를 견딜 수 있습니다.
유리-세라믹은 대부분의 해변 모래에서 발견되는 결정 (예를 들어, 석영) 알갱이에 번개가 칠 때 자연적으로 발생할 수도 있습니다. 이 경우에서, 번개의 극단적이고 즉각적인 열 (~2500 °C)은 융합을 통해 풀구라이트라고 하는 속이 빈 가지 모양의 뿌리 구조를 생성합니다.
Organic solids
유기 화학은 질소, 산소, 및 할로겐: 불소 염소, 브롬, 및 요오드와 같은 많은 다른 원소를 포함할 수 있는 탄소와 수소의 화합물의 구조, 속성, 구성, 반응, 및 합성 (또는 다른 수단)에 의한 준비를 연구합니다. 일부 유기 화합물에는 인 또는 황 원소가 포함될 수도 있습니다. 유기 고체의 예로는 목재, 파라핀 왁스, 나프탈렌, 및 다양한 폴리머와 플라스틱이 있습니다.
Wood
나무는 주로 리그닌(lignin)의 매트릭스에 삽입된 셀룰로오스(cellulose) 섬유로 구성된 천연 유기 재료입니다. 기계적 속성과 관련하여, 섬유는 장력이 강하고, 리그닌 매트릭스는 압축에 저항합니다. 따라서, 나무는 인간이 대피소를 짓고 보트를 사용하기 시작한 이래로 중요한 건축 자재였습니다. 건설 작업에 사용되는 목재는 일반적으로 목재 또는 목재로 알려져 있습니다. 건축에서 나무는 구조재일 뿐만 아니라 콘크리트의 거푸집을 형성하는 데에도 사용됩니다.
나무-기반 재료는 정제된 펄프에서 생성되는 포장 (예를 들어, 판지)와 종이에도 광범위하게 사용됩니다. 화학적 펄프화 공정은 리그닌을 연소시키기 전에 리그닌의 화학적 결합을 끊기 위해 고온 및 알칼리성 (크래프트) 또는 산성 (아황산염) 화학물질을 조합하여 사용합니다.
Polymers

유기 화학에서 탄소의 중요한 속성 중 하나는 특정 화합물을 형성할 수 있다는 것이며, 그것의 개별 분자는 서로 결합하여, 사슬이나 네트워크를 형성할 수 있습니다. 그 과정은 중합과 중합체의 체인 또는 네트워크라고 불리고, 반면에 원천 화합물은 단위체입니다. 두 가지 주요 중합체 그룹이 존재합니다: 인위적으로 제조된 중합체는 산업용 중합체 또는 합성 중합체 (플라스틱)이라고 참조되고 자연적으로 발생하는 중합체는 바이오폴리머입니다.
단위체는 용해도와 화학 반응성과 같은 유기 화합물의 화학적 특성뿐만 아니라 경도, 밀도, 기계적 또는 인장 강도, 내마모성, 열 저항성, 투명성, 색상 등과 같은 물리적 속성에 영향을 줄 수 있는 다양한 화학적 치환기 또는 작용기를 가질 수 있습니다. 단백질에서, 이들 차이는 중합체가 다른 것보다 우선적으로 생물학적 활성 형태를 채택할 수 있는 능력을 부여합니다 (self-assembly 참조).

사람들은 열가소성 중합체로 분류되는 왁스와 셸락(shellac) 형태로 수세기 동안 천연 유기 중합체를 사용해 왔습니다. 셀룰로오스(cellulose)라고 이름-지은 식물 중합체는 천연 섬유와 로프의 인장 강도를 제공했고, 19세기 초까지 천연 고무가 널리 사용되었습니다. 중합체는 공통적으로 플라스틱이라고 불리는 것을 만들기 위해 사용되는 원료 (수지)입니다. 플라스틱은 하나 이상의 중합체 또는 첨가제가 처리 중에 수지에 추가된 후 최종 형태로 형성된 최종 제품입니다. 주변에 있었고 현재 널리 사용되고 있는 중합체에는 탄소 기반 폴리에틸렌, 폴리프로필렌, 폴리염화비닐, 폴리스티렌, 나일론, 폴리에스테르, 아크릴, 폴리우레탄, 및 폴리카보네이트, 실리콘-기반 실리콘이 포함됩니다. 플라스틱은 일반적으로 "일용품", "특수", 및 "엔지니어링" 플라스틱으로 분류됩니다.
Composite materials


합성물 재료는 두 개 이상의 거시적 상을 포함하며, 그 중 하나는 종종 세라믹입니다. 예를 들어, 연속 매트릭스, 및 세라믹 입자 또는 섬유의 분산 상.
합성물 재료의 적용 범위는 철근 콘크리트와 같은 구조적 원소에서 지구 대기로 재진입하는 열로부터 셔틀 표면을 보호하기 위해 사용되는 NASA의 우주 왕복선 열 보호 시스템에서 핵심적이고 필수적인 역할을 하는 단열 타일에 이르기까지 다양합니다. 한 가지 예는 최대 1510°C (2750°F)의 재진입 온도를 견디고 우주 왕복선 날개의 노즈 캡과 앞쪽 가장자리를 보호하는 밝은 회색 소재인 강화 탄소-탄소 (RCC)입니다. RCC는 흑연 레이온 천으로 만들어지고 페놀 수지가 함침된 적층 복합 재료입니다. 오토클레이브에서 고온 경화 후, 라미네이트를 열분해하여 수지를 탄소로 전환시키고, 진공 챔버에서 푸르푸랄 알코올로 함침시키고, 푸르푸랄 알코올을 탄소로 전환시키기 위해 경화/열분해합니다. 재사용 기능을 위한 내산화성을 제공하기 위해 RCC의 외부 레이어는 탄화규소로 변환됩니다.
합성물의 국내 예는 텔레비전 세트, 휴대폰 등의 "플라스틱" 케이스에서 볼 수 있습니다. 이들 플라스틱 케이싱은 보통 아크릴로니트릴 부타디엔 스티렌 (ABS)과 같은 열가소성 매트릭스로 구성된 합성물이며 여기에는 탄산칼슘 초크, 활석, 유리 섬유 또는 탄소 섬유가 강도, 벌크 또는 정전기 분산을 위해 추가되었습니다. 이들 첨가물은 목적에 따라 강화 섬유 또는 분산제로 불릴 수 있습니다.
따라서, 매트릭스 재료는 상대 위치를 유지함으로써 보강 재료를 둘러싸고 지지합니다. 보강재는 특수한 기계적 및 물리적 속성을 부여하여 매트릭스 속성을 향상시킵니다. 시너지 효과는 개별 구성 재료에서 사용할 수 없는 재료 속성을 생성하는 반면, 다양한 매트릭스 및 보강 재료는 설계자가 최적의 조합을 선택할 수 있도록 합니다.
Semiconductors

반도체는 금속 전도체와 비금속 절연체 사이의 전기 저항 (및 전도성)을 가지는 물질입니다. 그것들은 붕소에서 오른쪽으로 대각선 아래로 이동하는 주기율 테이블에서 찾을 수 있습니다. 그것들은 절연체 (오른쪽)에서 전기 전도체 (또는 금속, 왼쪽)를 분리합니다.
반도체 재료로 만든 장치는 라디오, 컴퓨터, 전화 등 현대 전자 장치의 토대입니다. 반도체 장치에는 트랜지스터, 태양 전지, 다이오드, 및 집적 회로가 포함됩니다. 태양광 패널은 빛을 전기 에너지로 직접 변환하는 대형 반도체 소자입니다.
금속 전도체에서, 전류는 전자의 흐름에 의해 전달되지만, 반도체에서, 전류가 전자에 의해 또는 재료의 전자 밴드 구조에 있는 양전하 "정공"에 의해 전달될 수 있습니다. 공통적인 반도체 재료에는 실리콘, 게르마늄, 및 갈륨 비소가 포함됩니다.
Nanomaterials
많은 전통적인 고체는 나노미터 크기로 축소될 때 다른 속성을 나타냅니다. 예를 들어, 보통 노란색 금색과 회색 실리콘의 나노입자는 빨간색입니다; 금 나노입자는 금 슬래브 (1064°C)보다 훨씬 낮은 온도 (2.5nm 크기에 대해 ~300°C)에서 녹습니다;[10] 그리고 금속 나노와이어는 상응하는 벌크 금속보다 훨씬 강합니다.[11][12] 나노 입자의 높은 표면 넓이는 에너지 분야에서 특정 응용 분야에 매우 매력적입니다. 예를 들어, 백금 금속은 자동차 연료 촉매 및 양성자 교환막 (PEM) 연료 전지로서 개선을 제공할 수 있습니다. 역시, 란탄, 세륨, 망간, 및 니켈의 세라믹 산화물 (또는 서멧)은 현재 고체 산화물 연료 전지 (SOFC)로 개발되고 있습니다. 리튬, 리튬-티타네이트, 및 탄탈륨 나노입자가 리튬 이온 배터리에 적용되고 있습니다. 실리콘 나노입자는 확장/수축 주기 동안 리튬 이온 배터리의 저장 용량을 극적으로 확장하는 것으로 나타났습니다. 실리콘 나노와이어는 상당한 열화 없이 순환하며 저장 시간이 크게 연장된 배터리에 사용할 가능성을 제시합니다. 실리콘 나노입자는 새로운 형태의 태양 에너지 전지에도 사용되고 있습니다. 광기전 (태양) 셀의 다결정 실리콘 기판에 실리콘 양자점을 박막 증착하면 캡처 전에 들어오는 빛을 형광 처리하여 전압 출력을 60%까지 증가시킵니다. 여기에서도, 나노입자(및 박막)의 표면적은 흡수된 방사선의 양을 최대화하는 데 중요한 역할을 합니다.
Biomaterials
많은 천연 (또는 생물학적) 재료는 뛰어난 기계적 속성을 지닌 복합 복합물입니다. 수억 년의 진화를 통해 생겨난 이러한 복잡한 구조는 재료 과학자들에게 새로운 재료 설계에 영감을 주고 있습니다. 정의 특성에는 구조적 계층 구조, 다기능성, 및 자가 치유 기능이 포함됩니다. 자기-조직화는 역시 많은 생물학적 물질의 토대적인 특징이고 구조가 분자 수준에서 위로 조립되는 방식입니다. 따라서, 자기-조립(self-assembly)은 고성능 생체재료의 화학적 합성에서 새로운 전략으로 떠오르고 있습니다.
Physical properties
화학 합성의 결정적인 증거를 제공하는 원소와 화합물의 물리적 속성에는 냄새, 색상, 부피, 밀도 (단위 부피당 질량), 녹는 점, 끓는 점, 열 용량, 실온에서의 물리적 형태와 모양 (고체, 액체 또는 기체; 정육면체, 삼각 결정 등), 경도, 다공성, 굴절률, 및 기타 여러 가지가 포함됩니다. 이 섹션에서는 고체 상태에서 재료의 일부 물리적 속성에 대해 설명합니다.
Mechanical

재료의 기계적 속성은 강도와 변형 저항과 같은 특성을 설명합니다. 예를 들어, 강철 빔은 강도가 높기 때문에 건설에 사용되며, 그것들은 적용된 하중에서 심하게 파손되거나 구부러지지 않음을 의미합니다.
기계적 속성에는 탄성, 가소성, 인장 강도, 압축 강도, 전단 강도, 파괴 인성, 연성 (취성 재료가 낮음), 및 압입 경도가 포함됩니다. 고체 역학은 외부 힘과 온도 변화와 같은 외부 작용 아래에서 고체 물질의 행동을 연구하는 학문입니다.
고체는 유체처럼 거시적 흐름을 나타내지 않습니다. 원래 모양에서 임의의 벗어나는 정도는 변형(deformation)이라고 불립니다. 원래 크기에 대한 변형의 비율은 변형률(strain)이라고 불립니다. 만약 적용된 응력(stress)이 충분히 낮으면, 거의 모든 고체 재료가 변형이 응력에 직접 비례하는 방법으로 행동합니다 (훅의 법칙(Hooke's law)). 비율의 계수는 탄성의 모듈러스(modulus of elasticity) 또는 영의 모듈러스(Young's modulus)라고 불립니다. 이 변형 영역은 선형 탄성(linearly elastic) 영역으로 알려져 있습니다. 고체가 적용된 응력에 반응하는 방법을 세 가지 모델로 설명할 수 있습니다:
- 탄성(Elasticity) – 적용된 응력이 제거될 때, 재료가 변형되지 않은 상태로 돌아갑니다.
- 점탄성(Viscoelasticity) – 이것들은 탄력적으로 행동하지만, 감쇠(damping)도 있는 재료입니다. 적용된 응력이 제거될 때, 감쇠 효과에 대한 작업을 수행해야 하고 재료 내에서 열로 변환됩니다. 그 결과 응력-변형률 곡선에 히스테리시스 루프(hysteresis loop)가 생깁니다. 이것은 기계적 응답이 시간-의존성을 가진다는 것을 의미합니다.
- 가소성(Plasticity) – 탄성적으로 행동하는 재료는 일반적으로 적용된 응력이 항복 값보다 작을 때 그렇게 합니다. 응력이 항복 응력보다 클 때, 재료는 소성 행동을 하고 이전 상태로 돌아가지 않습니다. 즉, 비가역적인 소성 변형 (또는 점성 유동)은 영구적인 항복 이후에 발생합니다.
많은 재료는 높은 온도에서 약해집니다. 높은 온도에서 강도를 유지하는 내화 재료(refractory materials)라고 하는 재료는 많은 목적에 유용합니다. 예를 들어, 유리-세라믹은 우수한 기계적 속성을 나타내고 최대 1000°C까지 반복적이고 빠른 온도 변화를 견딜 수 있기 때문에 조리대 요리에 매우 유용합니다. 항공-우주 산업에서, 항공기 및/또는 우주선 외장 설계에 사용되는 고성능 재료는 열 충격에 대한 저항성이 높아야 합니다. 따라서, 유기 중합체와 중합체/세라믹/금속 복합 재료 및 섬유 강화 중합체로 만든 합성 섬유는 이제 이러한 목적을 염두에 두고 설계되고 있습니다.
Thermal

고체는 열 에너지를 가지고 있기 때문에, 그것들의 원자는 순서화된 (또는 비-순서화된) 격자 내에서 고정된 평균 위치에 대해 진동합니다. 결정질 또는 유리질 네트워크에서 격자 진동의 스펙트럼은 고체 운동 이론(kinetic theory of solids)의 토대를 제공합니다. 이 움직임은 원자 수준에서 발생하고, 따라서 분광기에 사용되는 것과 같은 고도로 전문화된 장비 없이는 관찰하거나 감지할 수 없습니다.
고체의 열적 속성에는 열을 전도하는 능력을 나타내는 재료의 속성인 열 전도성(thermal conductivity)이 포함됩니다. 고체는 역시 열 (또는 열 격자 진동)의 형태로 에너지를 저장하기 위한 재료의 용량인 특정 열 용량(specific heat capacity)을 가지고 있습니다.
Electrical
전기적 속성에는 전기 저항과 전도성, 유전 강도, 전자기 투자율, 및 유전율이 모두 포함됩니다. 금속과 합금과 같은 전기 전도체는 유리와 세라믹과 같은 전기 절연체와 대조됩니다. 반도체는 그 중간 어딘가에서 작동합니다. 금속에서 전도성은 전자에 의해 발생하는 반면, 전자와 정공은 모두 반도체의 전류에 기여합니다. 대안적으로, 이온은 이온 전도체에서 전류를 지원합니다.
많은 물질은 역시 낮은 온도에서 초전도성(superconductivity)을 나타냅니다. 여기에는 주석 및 알루미늄과 같은 금속 원소, 다양한 금속 합금, 일부 강하게 도핑된 반도체 및 특정 세라믹이 포함됩니다. 대부분의 전기 (금속) 전도체의 전기 저항은 일반적으로 온도가 낮아짐에 따라 점진적으로 감소하지만 유한한 상태를 유지합니다. 어쨌든, 초전도체에서는 재료가 임계 온도 이하로 냉각되면 저항이 갑자기 영으로 떨어집니다. 초전도선의 고리에 흐르는 전류는 전원이 없어도 무한정 지속될 수 있습니다.
유전체(dielectric), 또는 전기 절연체는 전류의 흐름에 매우 강한 물질입니다. 플라스틱과 같은 유전체는 인가된 전기장을 자체 내부에 집중시키는 경향이 있으며, 이러한 속성은 콘덴서에 사용됩니다. 콘덴서는 밀접하게 간격을 둔 한 쌍의 도체 ('플레이트'라고 함) 사이의 전기장에 에너지를 저장할 수 있는 전기 장치입니다. 콘덴서에 전압이 가해질 때, 크기는 같지만 극성이 반대인 전하가 각 판에 쌓입니다. 콘덴서는 고주파 신호와 저주파 신호를 구별하기 위한 전자 필터뿐만 아니라 에너지 저장 장치로 전기 회로에 사용됩니다.
Electro-mechanical
압전성(Piezoelectricity)은 인가된 기계적 응력에 반응하여 전압을 생성하는 결정의 능력입니다. 압전 효과는 해당 압전 결정체에서, 외부에서 인가된 전압이 가해질 때, 미량의 형태로 변형될 수 있다는 점에서 가역적입니다. 고무, 양모, 머리카락, 나무 섬유, 및 실크와 같은 고분자 재료는 종종 일렉트릿(electrets)처럼 작동합니다. 예를 들어, 중합체 폴리비닐리덴 플루오라이드(polyvinylidene fluoride, PVDF)는 전통적인 압전 재료 석영 (결정질 SiO2)보다 몇 배 더 큰 압전 응답을 나타냅니다. 변형 (~0.1%)은 고전압 소스, 라우드스피커, 레이저뿐만 아니라, 화학적, 생물학적, 및 음향-광학 센서 및/또는 트랜스듀서와 같은 유용한 기술 응용 분야에 적합합니다.
Optical
재료는 가시반직선을 투과 (예를 들어, 유리)하거나 반사 (예를 들어, 금속)할 수 있습니다.
많은 재료는 일부 파장을 투과시키면서 다른 파장은 차단합니다. 예를 들어, 창문 유리는 가시 반직선(visible light)에는 투명하지만 일광화상(sunburn)의 원인이 되는 대부분의 자외선 주파수에는 훨씬 덜 투명합니다. 이 속성은 입사 빛의 색상을 변경할 수 있는 주파수 선택적 광학 필터에 사용됩니다.
어떤 목적에 대해, 재료의 광학적 속성과 기계적 속성이 모두 관심 대상이 될 수 있습니다. 예를 들어, 적외선 호밍 ("열-추적") 미사일의 센서는 적외선 방사(infrared radiation)에 투명한 덮개로 보호되어야 합니다. 현재 고속 적외선 유도 미사일 돔에 사용되는 재료는 단결정 사파이어입니다. 사파이어의 광학 전송은 전체 중간-적외선 범위 (3–5µm)를 덮을 수 있도록 실제로 확장되지 않지만 실온에서 약 4.5µm보다 큰 파장에서 떨어지기 시작합니다. 사파이어의 강도는 실온에서 사용 가능한 다른 중급 적외선 돔 재료보다 우수하지만 600°C 이상에서는 약해집니다. 광 대역 통과와 기계적 내구성 사이에는 오랜 트레이드오프가 존재합니다. 투명 세라믹 또는 광학 나노복합체와 같은 신소재는 향상된 성능을 제공할 수 있습니다.
유도된 빛-파장 전송은 광섬유 분야와 그것들 사이의 작은 간섭을 갖는 주파수 범위 (다중 모드 광학 도파관)를 동시에 및 낮은 강도 손실로 전송하기 위한 특정 유리질의 능력을 포함합니다. 광 도파관은 집적 광 회로의 구성 요소 또는 광 통신 시스템의 전송 매체로 사용됩니다.
Opto-electronic
태양 전지 또는 광전지는 빛 에너지를 전기 에너지로 변환하는 장치입니다. 토대적으로, 그 장치는 두 가지 기능만 수행하면 됩니다: 광 흡수 물질에서 전하 운반체 (전자와 정공)의 광 생성 및 전기를 전달하는 전도성 접촉부로 전하 운반체를 분리합니다(간단히 말하면 금속 접촉부를 통해 전자를 외부 회로로 운반합니다). 이러한 변환은 광전 효과(photoelectric effect)라고 불리고, 태양 전지와 관련된 연구 분야를 광전지(photovoltaics)라고 알려져 있습니다.
태양 전지에는 많은 응용 분야가 있습니다. 그것들은 원격 지역 전력 시스템, 지구 궤도 위성과 우주 탐사선, 휴대용 계산기, 손목 시계, 원격 무선 전화, 및 물 펌핑 응용 프로그램과 같이 그리드의 전력을 사용할 수 없는 상황에서 오랫동안 사용되어 왔습니다. 최근에는 인버터를 통해 전기 그리드에 연결된 태양광 모듈 (태양광 어레이) 어셈블리에 사용되기 시작했습니다.
모든 태양 전지는 광자를 흡수하고 광전 효과를 통해 전자를 생성하기 위해 전지 구조 내에 포함된 광 흡수 재료가 필요합니다. 태양 전지에 사용되는 물질은 지구 표면에 도달하는 태양광의 파장을 우선적으로 흡수하는 성질을 가지는 경향이 있습니다. 일부 태양 전지는 지구 대기권 너머의 광 흡수에도 최적화되어 있습니다.
References
- ^ Holley, Dennis (2017-05-31). GENERAL BIOLOGY I: Molecules, Cells and Genes. Dog Ear Publishing. ISBN 9781457552748.
- ^ Rogers, Ben; Adams, Jesse; Pennathur, Sumita (2014-10-28). Nanotechnology: Understanding Small Systems, Third Edition. CRC Press. ISBN 9781482211726.
- ^ Nahum, Alan M.; Melvin, John W. (2013-03-09). Accidental Injury: Biomechanics and Prevention. Springer Science & Business Media. ISBN 9781475722642.
- ^ Narula, G. K.; Narula, K. S.; Gupta, V. K. (1989). Materials Science. Tata McGraw-Hill Education. ISBN 9780074517963.
- ^ Arnold, Brian (2006-07-01). Science Foundation. Letts and Lonsdale. ISBN 9781843156567.
- ^ Group, Diagram (2009-01-01). The Facts on File Chemistry Handbook. Infobase Publishing. ISBN 9781438109558.
- ^ Mortimer, Charles E. (1975). Chemistry: A Conceptual Approach (3rd ed.). New York: D. Van Nostrad Company. ISBN 0-442-25545-4.
- ^ Bar-Cohen, Yoseph; Zacny, Kris (2009-08-04). Drilling in Extreme Environments: Penetration and Sampling on Earth and other Planets. John Wiley & Sons. ISBN 9783527626632.
- ^ "Ceramics". autocww.colorado.edu. Archived from the original on 17 July 2019.
- ^ Buffat, Ph.; Borel, J.-P. (1976). "Size effect on the melting temperature of gold particles". Physical Review A. 13 (6): 2287. Bibcode:1976PhRvA..13.2287B. doi:10.1103/PhysRevA.13.2287.
- ^ Walter H. Kohl (1995). Handbook of materials and techniques for vacuum devices. Springer. pp. 164–167. ISBN 1-56396-387-6.
- ^ Shpak, Anatoly P.; Kotrechko, Sergiy O.; Mazilova, Tatjana I; Mikhailovskij, Igor M (2009). "Inherent tensile strength of molybdenum nanocrystals". Science and Technology of Advanced Materials. 10 (4): 045004. Bibcode:2009STAdM..10d5004S. doi:10.1088/1468-6996/10/4/045004. PMC 5090266. PMID 27877304.
External links